DOI: 10.1021/acsinfecdis.0c00321
一半以上的糖尿病傷口表現出感染的臨床癥狀,且預后不良。本研究旨在研制一種可負載生物活性抗生素和血小板衍生生長因子(PDGF)的同軸芯鞘聚乳酸-乙交酯(PLGA)納米纖維支架,用于糖尿病感染創面的修復。將PDGF和PLGA/抗生素溶液分別泵入兩個獨立的毛細管內進行同軸靜電紡絲,以制備可生物降解的芯鞘納米纖維。紡制的納米纖維支架可持續釋放PDGF、萬古霉素和慶大霉素長達三周。該支架降低了磷酸酶和張力蛋白同源物的含量,增加了創面周圍血管生成標志物(CD31)的含量,促進了感染性糖尿病創面修復的早期愈合。載有抗生素/生物分子的PLGA納米纖維為感染性糖尿病傷口部位的組織再生提供了一種非常有效的方法。
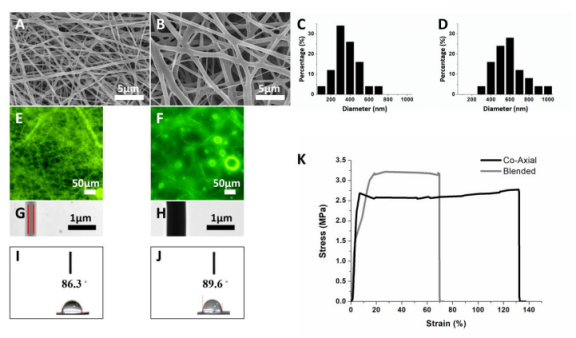
圖1.同軸和混合納米纖維膜的特性。芯鞘(A)和混合(B)電紡納米纖維的電子顯微鏡掃描照片(比例尺:5μm)。提供兩組直徑的分布(C-D);同軸納米纖維和混合納米纖維的平均直徑分別為371±162nm和655±206nm。激光掃描共聚焦顯微鏡(E-F)對reGFP的觀察顯示,芯鞘組的線狀reGFP密度高于混合組。透射電子顯微鏡圖像顯示在芯鞘組(G)中有兩種密度(紅線之間),而在混合處理組(H)中沒有。同軸(I)組和混合(J)組中測得的接觸角分別為86.3°和89.6°,并且沒有顯著差異(p=0.077)。同軸和混合PLGA納米纖維支架的應力-應變曲線(K);底部軌跡為rhPDGF-BB或PBS/抗生素/PLGA支架,極限抗拉強度為2.78MPa,斷裂應變為129.89%;頂部軌跡為混合抗生素/PLGA支架,極限抗拉強度為3.22MPa,斷裂應變為67.7%。
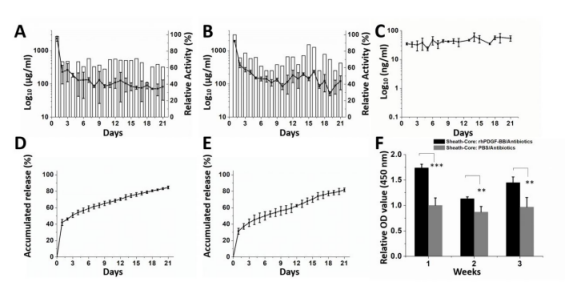
圖2.萬古霉素(A),慶大霉素(B)和rhPDGF-BB(C)在芯鞘納米纖維膜中的體外釋放行為和生物活性。三周的釋放模式,顯示從第1天(萬古霉素:2330±414μg/ml;慶大霉素:1946±104μg/ml)到第21天(萬古霉素:82±50μg/ml;慶大霉素:121±55μg/ml)穩定釋放。在三周期間,兩種濃度均超過最小抑菌濃度(20μg/ml),并且對金黃色葡萄球菌和大腸桿菌的生物活性均超過40%。直到第21天釋放的rhPDGF-BB濃度(54.6.1±11.4ng/ml)才發生波動,范圍從23.6ng/ml(第5天)至62.7ng/ml(第14天)。第21天萬古霉素(D)和慶大霉素(E)的累積釋放分別為84.6±1.7%和81.6±2.2%。第1、2和3周釋放的rhPDGF-BB洗脫液的生物活性顯著改善了成纖維細胞的增殖(F)(**p<0.01;***p<0.001)。
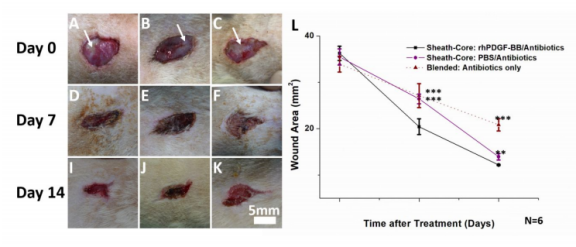
圖3.金黃色葡萄球菌和大腸桿菌溫育24小時后,感染性糖尿病傷口不同天數的治療情況(比例尺=5mm)。第0天注意到白色膿樣物質(白色箭頭),表明傷口被細菌感染(A-C)。rhPDGF-BB組(A,D和I)的傷口恢復速度比不含rhPDGF-BB的同軸組(B,E和J)和僅含抗生素的混合組(C,F和K)的傷口恢復快(L)(**=p<0.01;***=p<0.001)。
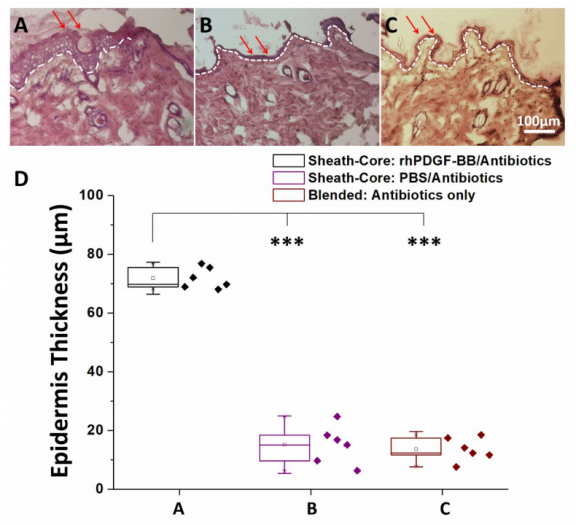
圖4.第14天三組糖尿病傷口的組織學顯微鏡圖像(A,B和C)(比例尺=100μm);rhPDGF-BB組的表皮厚度最大(D)(***=事后p<0.001)。
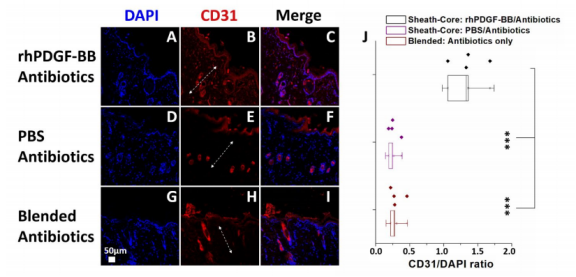
圖5.在含芯鞘rhPDGF-BB/抗生素(A,B和C),PBS/抗生素(D,E和F)以及僅混合抗生素(G,H和I)的不同組中,抗CD31抗體在糖尿病感染傷口上的免疫熒光顯微鏡圖像(比例尺=50μm)。rhPDGF-BB組真皮(雙箭頭)中CD31與DAPI的比值最高(B,E和H)(J)(***=p<0.001)。
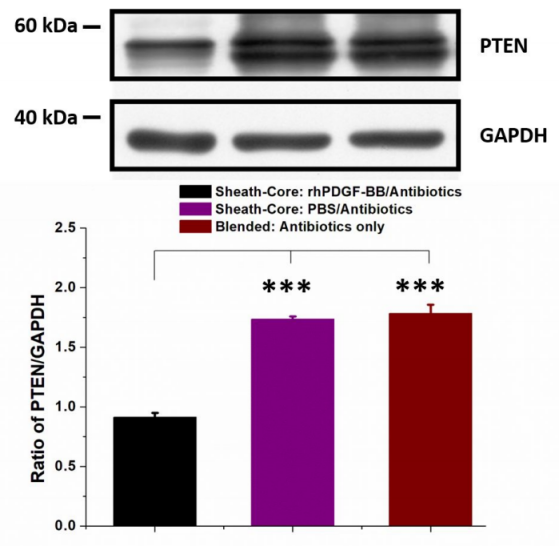
圖6.第2周傷口區域中PTEN的蛋白質印跡。芯鞘rhPDGF-BB/抗生素/PLGA組的PTEN與GAPDH的比值低于芯鞘PBS/抗生素/PLGA組以及僅含抗生素的混合PLGA組(***=p<0.001)。
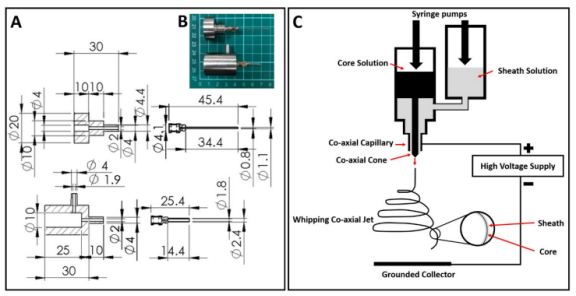
圖7.用于電紡同軸芯鞘納米纖維的裝置。(A)同軸靜電紡絲針的設計。(B)同軸針。(C)同軸靜電紡絲工藝示意圖。