DOI:10.1016/j.msec.2020.110936
與傷口愈合過程相關的致病性細菌感染通常會導致嚴重的并發癥。在本文中,制備了具有光動力治療(PDT)效果的生物相容性抗菌電紡納米纖維墊,以加速感染傷口的愈合。通過對水溶液中聚陰離子聚(γ-谷氨酸)(γ-PGA)和陽離子光敏劑5,10,15,20-四(1-甲基-4-吡啶基)卟啉四(對甲苯磺酸鹽)(TMPyP)的共靜電紡絲制備了納米纖維墊,并通過化學交聯使其穩定。所制備的納米纖維墊不僅能為傷口床提供濕潤的微環境,而且還可以通過釋放細胞毒性的活性氧(ROS)在可見光照射下提供有效的殺菌活性。體外抗菌試驗表明,在較低的TMPyP負載量(0.1 wt%)下,它們能有效地消除板譜細菌。同時,這些納米纖維墊表現出良好的生物相容性,對哺乳動物細胞和紅細胞(RBCs)沒有明顯的不利影響。體內動物試驗表明,及時有效的抗菌治療具有可忽略的局部毒性,可以達到抑制炎癥反應和促進傷口愈合的目的。這種具有生物相容性和抗菌性的γ-PGA-TMPyP納米纖維墊在實際的抗感染應用,尤其是傷口敷料應用中,顯示出巨大的潛力。
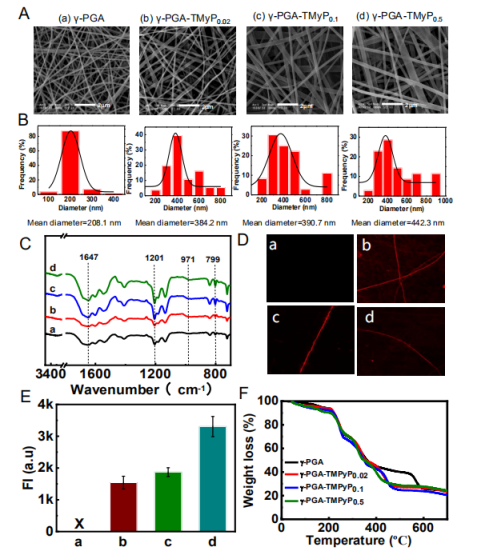
圖1.制備的納米纖維墊交聯前的特性。(A)(a)γ-PGA、(b)γ-PGA-TMPyP0.02、(c)γ-PGA-TMPyP0.1和(d)γ-PGA-TMPyP0.5的代表性SEM圖像。(B)相應納米纖維墊的直徑分布。(C)各種納米纖維交聯之前的ATR-FTIR光譜。(D)具有不同TMPyP含量的各種納米纖維墊的熒光強度統計。(E)墊中單納米纖維的代表性CLSM圖像。(F)不同納米纖維墊交聯之前的TGA曲線。
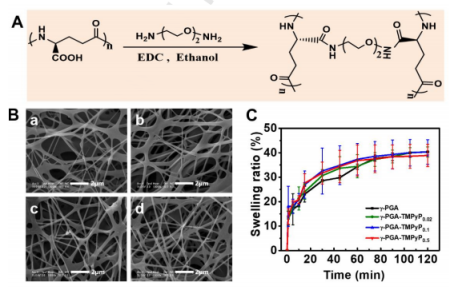
圖2.(A)γ-PGA與NH2-OEG2-NH2之間交聯反應的示意圖。(B)在PBS溶液中浸泡7天后的交聯納米纖維氈的代表性SEM圖像(a.γ-PGA,b.γ-PGA-TMPyP0.02,c.γ-PGA-TMPyP0.1,d.γ-PGA -TMPyP0.5)。(C)相應納米纖維墊的溶脹率。
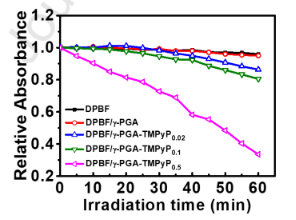
圖3.在不同時間間隔(0-60min)下,在光照射(650±10 nm)下與不同樣品孵育后,DPBF溶液的相對衰減吸收曲線。
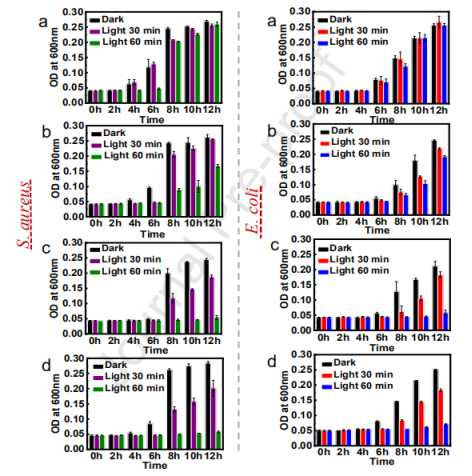
圖4.在一定的孵育時間間隔(a.γ-PGA、b.γ-PGA-TMPyP0.02、c.γ-PGA-TMPyP0.1和d.γ-PGA-TMPyP0.5)下,通過OD600 nm測量不同處理(黑暗、光照30min和60min)下納米纖維墊上殘留金黃色葡萄球菌和大腸桿菌的生長趨勢。
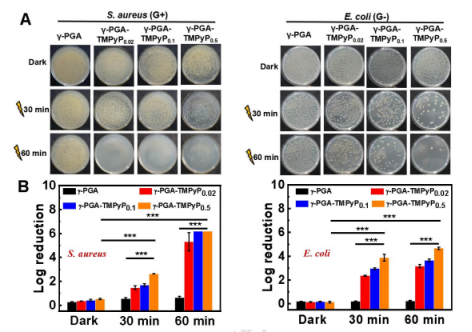
圖5.(A)在不同的抗菌處理(黑暗、30分鐘和60分鐘的光照)下,不同納米纖維墊上殘留的金黃色葡萄球菌和大腸桿菌的LB-瓊脂平板照片。(B)在輻照處理后,不同納米纖維墊細菌數目的相應對數減少。誤差線表示標準偏差(n=3)。
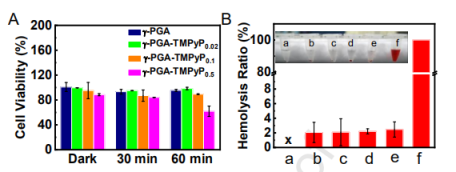
圖6.不同納米纖維墊的生物相容性評估。(A)在不同處理下與不同樣品孵育后的L929細胞生存力。(B)(a)正鹽、(b)γ-PGA、(c)γ-PGA-TMPyP0.02、(d)γ-PGA-TMPyP0.1、(e)γ-PGA-TMPyP0.5和(f)H2O的溶血活性。誤差線表示標準偏差(n=3)。
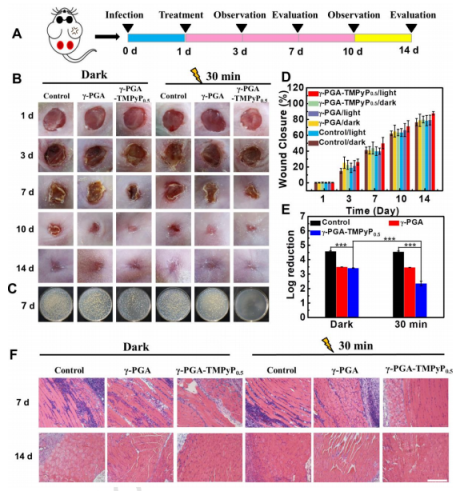
圖7.γ-PGA-TMPyP0.5納米纖維墊在金黃色葡萄球菌感染的小鼠傷口模型中作為抗感染傷口敷料的體內評估。 (A)建立小鼠傷口模型和治療過程的示意圖。 (B)不同治療后不同時間間隔(1、3、7、10、14天)的傷口典型照片。(C)從不同傷口組織收獲的細菌菌落的LB-瓊脂照片。(D)在愈合1-14天期間每個傷口的閉合率。(E)不同傷口組織的細菌菌落的對數減少。(F)H&E染色后金黃色葡萄球菌感染的傷口組織的組織學圖像。比例尺:50 μm。
 微信二維碼
微信二維碼