聚己內酯(PCL)作為一種潛在的生物降解材料也已被廣泛研究,它是由有機金屬化合物催化環狀單體ε-己內酯開環聚合而得到完全可生物降解的聚酯之一。PCL具有無免疫源性、降解過程不產生酸堆積、生物相容性好、柔韌性強、力學強度高、共混相容性好等諸多優點,這些優點使得PCL在生物醫用領域有著廣泛的應用。
1.Sci. Rep.:小檗堿/聚己內酯/膠原蛋白電紡支架的制備及其骨缺損修復能力

?南京大學林梓桐&劉超&苗雷英采用靜電紡絲法制備了含不同濃度小檗堿(BBR)(25、50、75和100μg/mL)的小檗堿/聚己內酯/膠原蛋白(BBR/PCL/COL)支架。
?BBR/PCL/COL支架在25-75μg/mL濃度范圍內具有良好的生物相容性,而50和75μg/mL的支架可顯著促進牙髓干細胞的成骨分化。
?將含50μg/mL BBR的支架植入大鼠臨界骨缺損處,以評估其體內骨修復的能力。結果表明,BBR/PCL/COL支架比聚己內酯/膠原蛋白(PCL/COL)支架具有更好的性能。
?首次評估了BBR/PCL/COL電紡支架的體內骨修復能力。結果表明,BBR/PCL/COL支架在組織工程骨再生治療中具有廣闊的應用前景。
DOI: 10.1038/s41598-020-79734-9
2.Int. J. Biol. Macromol.:含徑向互連大通道和定向納米纖維的3D礦化聚己內酯納米纖維支架的制備及其骨再生應用
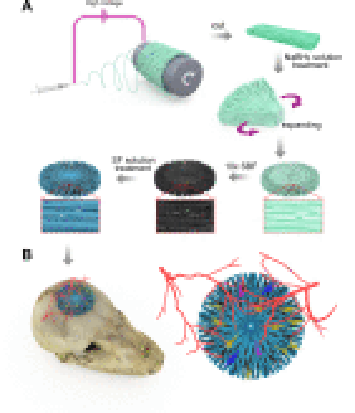
?武漢大學中南醫院蔡林研究開發了一種三維(3D)聚己內酯納米纖維支架,并通過生物礦化和絲素蛋白涂層對其進行修飾。
?該支架可以引導細胞排列,而徑向對齊的支架顯示出更強的促進細胞增殖的能力。體內結果表明,徑向對齊的支架可以引導組織的排列和重塑,并支持骨組織的快速再生。
?具有徑向互連大通道和定向納米纖維的3D礦化聚己內酯納米纖維支架有望用于組織工程,包括骨缺損、軟骨或其他復合組織的修復。
DOI: 10.1016/j.ijbiomac.2021.01.036
3. Mater. Sci. Eng. C:靜電紡絲超細聚合物纖維與生物活性陶瓷雜化物,用于骨組織再生
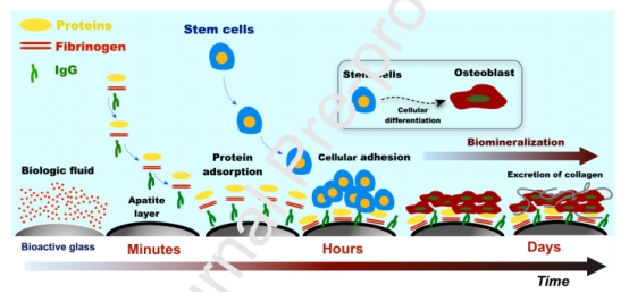
?介紹了電紡超細聚合物纖維與生物活性陶瓷雜化物的最新研究進展,重點在于其骨組織再生能力。
?本文綜述了生物活性陶瓷的制備方法,特別是納米羥基磷灰石(nano-HA)和生物活性玻璃(BG)的制備,它們是骨再生陶瓷的研究熱點。
?本文涵蓋了骨的解剖和力學特性以及基本的組織-支架相互作用機制。從技術角度、制備策略、工藝變量、表征方法和生物學要求(體外和體內性能)等方面詳細討論了電紡超細纖維的工藝-結構-性能關系。
?本文重點介紹了其主要挑戰和未來前景,為下一代骨組織工程雜化材料鋪平了道路。
DOI: 10.1016/j.msec.2020.111853
4. Mater. Sci. Eng. C:PCL/BMP-6@ZIF-8電紡纖維支架的制備及其骨再生應用
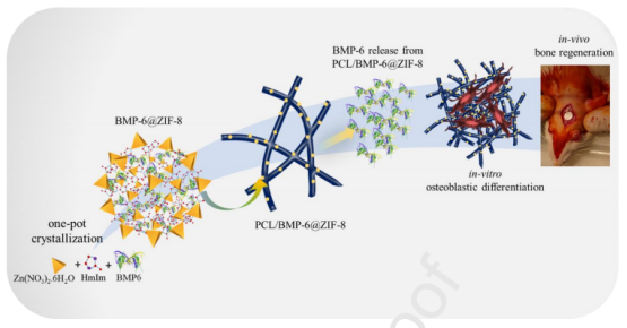
?首次開發了可控釋BMP-6的MOF嵌入電紡纖維支架,以增強骨再生功效。首先,將BMP-6包封ZIF-8納米晶體作為生長因子分子的新型載體,進行一步快速結晶,然后靜電紡絲由聚(ε-己內酯)和BMP-6包封ZIF-8納米晶體組成的混合溶液,從而制備出納米纖維支架。
?BMP-6的生物活性得以保留,釋放時間長達30天。釋放動力學符合Korsmeyer-Peppas模型,表現出偽Fickian行為。體外成骨研究表明BMP-6緩釋對MC3T3-E1前成骨細胞的成骨分化有明顯的促進作用。
?體內研究還顯示BMP-6的持續緩慢釋放是導致大鼠顱骨缺損中礦化良好的新骨形成的原因。該研究結果證實嵌入MOF載體的電紡支架可以用作骨組織工程應用中骨再生的有效平臺。
DOI:10.1016/j.msec.2020.111738
5. Appl. Mater. Today:Cu-Zn雙層納米纖維膜的雙時態雙向免疫調節作用可增強抗菌活性和成骨作用
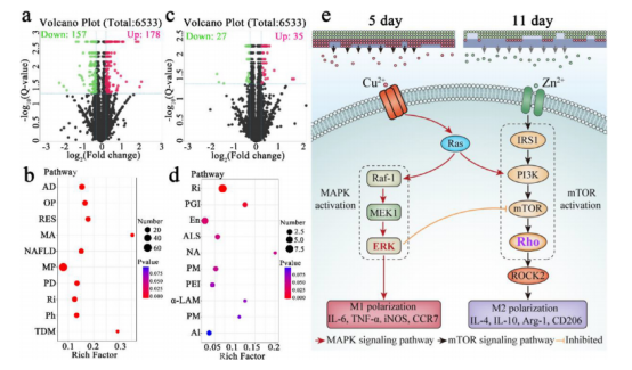
?上海交通大學附屬第六人民醫院沈灝&張先龍&中國科學院上海硅酸鹽研究所常江針對IRIs和種植體骨整合障礙的免疫學特征,研究者提出了一種序貫免疫調節策略來應對該類并發癥,使用由簡便的靜電紡絲工藝和熱壓法合成的Cu-Zn雙層納米纖維膜。
?Cu-Zn雙層納米纖維膜具有良好的Cu2+和Zn2+的受控釋放,并且可以通過交替激活MAPK和mTOR信號通路依次調節從M1到M2的巨噬細胞表型轉變。
?雙時態雙向免疫調節作用賦予了Cu-Zn雙層納米纖維膜在體外和體內優異的抗感染和成骨能力。這是第一種專門針對IRIs和種植體骨整合障礙的免疫要求而設計的雙時態雙向免疫調節生物材料。
DOI:10.1016/j.apmt.2020.100888
6. Adv. Funct. Mater.:具有直接成骨和骨免疫調節功能的分層Janus納米纖維膜的制備及其骨再生應用
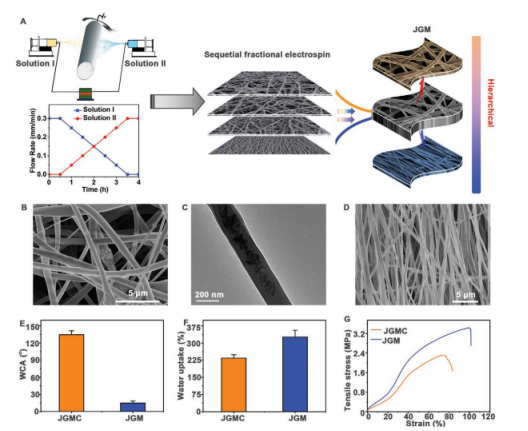
?四川大學趙偉鋒采用連續分步靜電紡絲法設計并制備了一種Janus GBRM(JGM)。將羥基磷灰石(HAP)負載隨機明膠纖維設計為內表面,以促進成骨細胞的粘附、增殖和成骨分化,同時將P(DMC-AMA)負載定向聚己內酯(PCL)納米纖維作為外層以抵抗上皮細胞入侵和細菌感染。
?內表面具有增強的成骨作用,同時外表面可調節上皮細胞沿排列方向擴散并殺死接觸的細菌。有趣的是,外表面可誘導巨噬細胞向M2表型極化,從而調控良好的骨免疫環境。
?JGM同時滿足屏障、成骨、抗菌和骨免疫調節功能的關鍵要求。與商用生物引導膜相比,JGM具有更好的體內骨組織再生性能。DOI: 10.1002/adfm.202008906
7. Processes:功能化電紡人工微環境的制備及其在骨組織再生中的應用
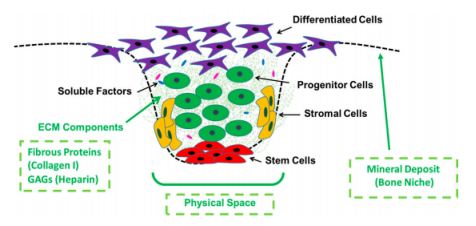
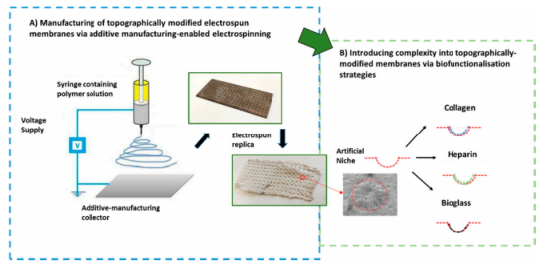
?在這項研究中,應用了三種方法來對空間受限的電紡人工微環境進行功能化,這些微環境呈現出天然骨干細胞巢的相關成分。
?在細胞外基質(ECM)蛋白(I型膠原蛋白)、糖胺聚糖(肝素)和陶瓷基材料(生物玻璃)功能化的電紡微加工支架上研究了間充質干細胞(MSCs)的生物學和成骨行為。
?在不改變聚己內酯(PCL)支架提供的纖維結構的前提下,成功地將膠原蛋白、肝素和生物玻璃(BG)納入模型中。間充質干細胞(MSCs)成功植入所有生物功能支架中,當暴露于PCL/BG復合材料中時,堿性磷酸酶生成量增加。
DOI:10.3390/pr8111341
 微信二維碼
微信二維碼