DOI:10.1016/j.carbpol.2020.116477
復雜的納米結構與碳水化合物聚合物的結合為促進新型藥物傳輸系統的發展提供一個強大的平臺。在這項研究中,以醋酸纖維素(CA)為關鍵纖維形成的聚合物基質,以酮洛芬(KET)為模型藥物,制備了具有離散藥物分布的三層核-殼型納米纖維F2。離散分布的特征是通過改進的三軸靜電紡絲技術在CA/KET核心層和PVP/KET外層之間插入無藥的CA空白層。與傳統的核-殼納米纖維F1相比, 具有藥物離散分布的三層納米纖維F2在第一階段的精確釋放所設計的藥物量,第二階段以較長時間調控藥物緩慢釋放,從而獲得精準的兩相控釋方式。盡管具有相同的成分(藥物、可溶性PVP和不溶性CA)和相似的線性形態,但核-殼納米纖維F1和三層納米纖維F2在提供雙階段釋放方面表現出明顯的差異。兩種類型納米纖維的不同結構-性能關系在控制雙階段藥物控釋曲線的準確性方面產生了不同的效果。論文對于含有空白CA中間層的三層核-殼結構準確調控藥物分子釋放行為的機理進行了分析。
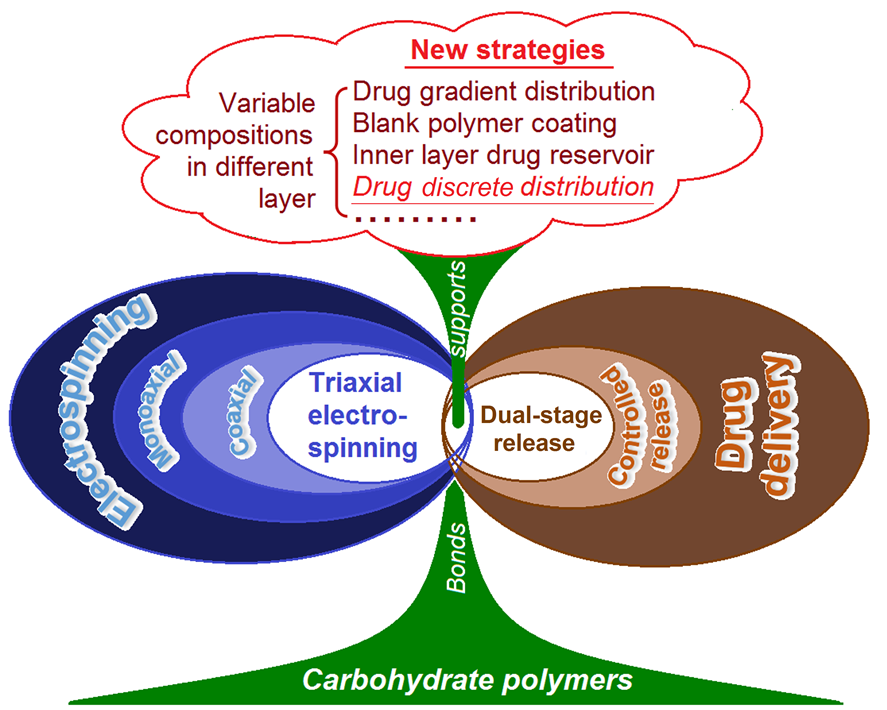
圖1.該圖顯示碳水化合物聚合物充當了先進技術和生物醫學應用的紐帶,并為實現不同的新策略提供了有力的支持。
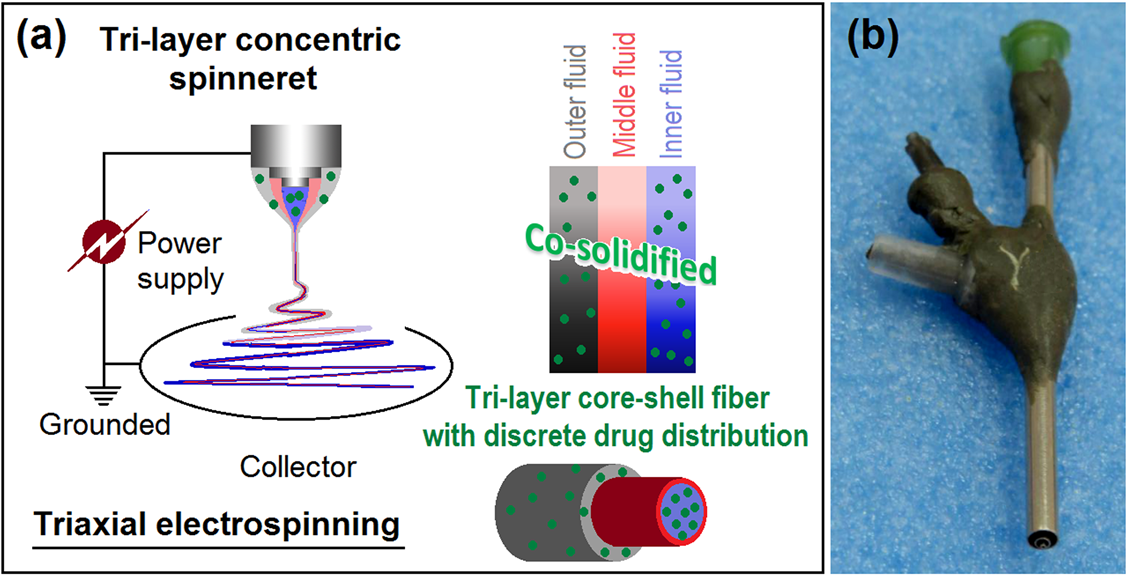
圖2.改進的三軸靜電紡絲示意圖,用于創建具有離散藥物分布的三層核-殼納米纖維(a)和本研究中應用的自制噴絲頭(b)。

圖3.改進的同軸和三軸靜電紡絲工藝的實現:(a)數字圖片,顯示了三種工作流體與噴絲頭的連接方式;(b)典型改進的同軸靜電紡絲工藝用于制備納米纖維F1,左上插圖顯示了核-殼復合泰勒錐;(c)典型改進的三軸靜電紡絲工藝用于產生具有離散藥物分布的納米纖維F2;(d)典型的三層核-殼泰勒錐。
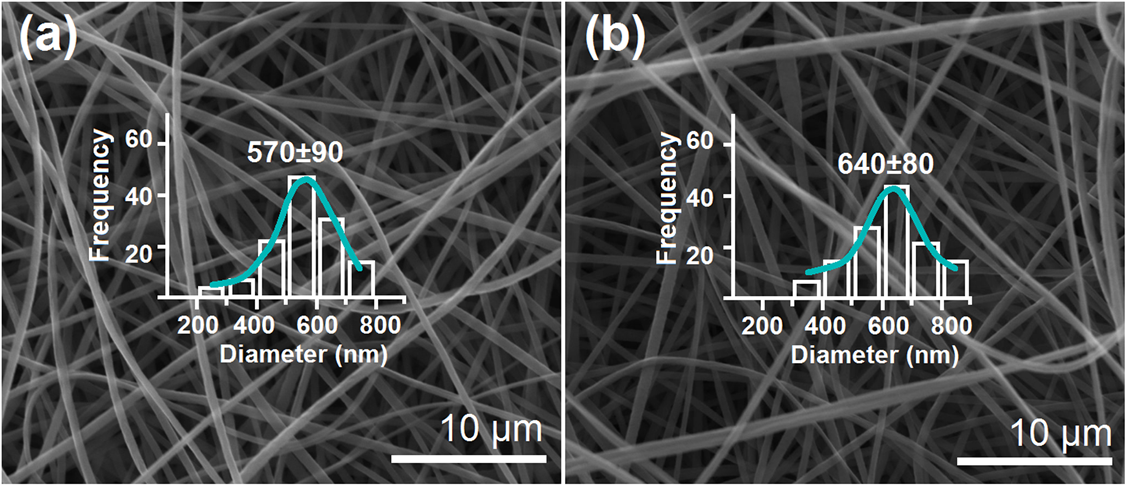
圖4.制備的纖維F1(a和b)和F2(c和d)的SEM圖像。

圖5.制備的纖維F1(a)和納米倉庫F2(b)的TEM圖像。
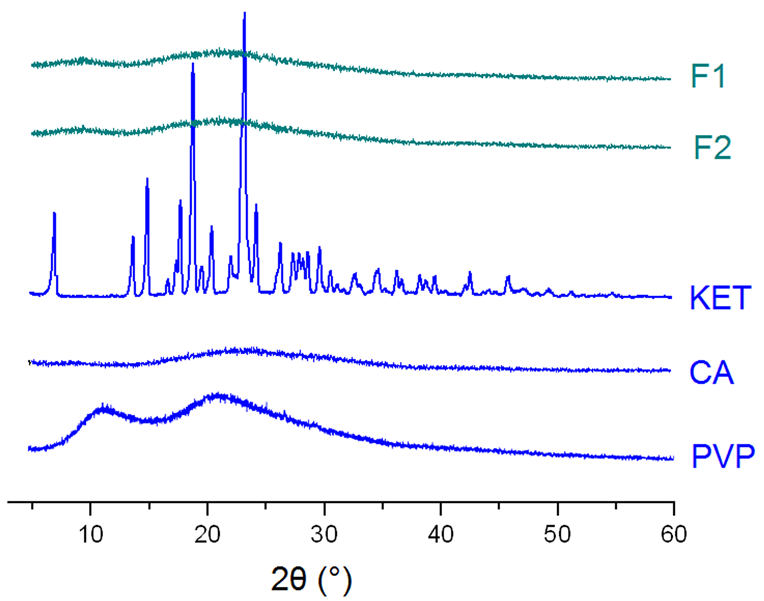
圖6.原料粉末(KET、PVP和CA)、核-殼納米纖維F1和三層核-殼納米纖維F2的XRD圖譜。
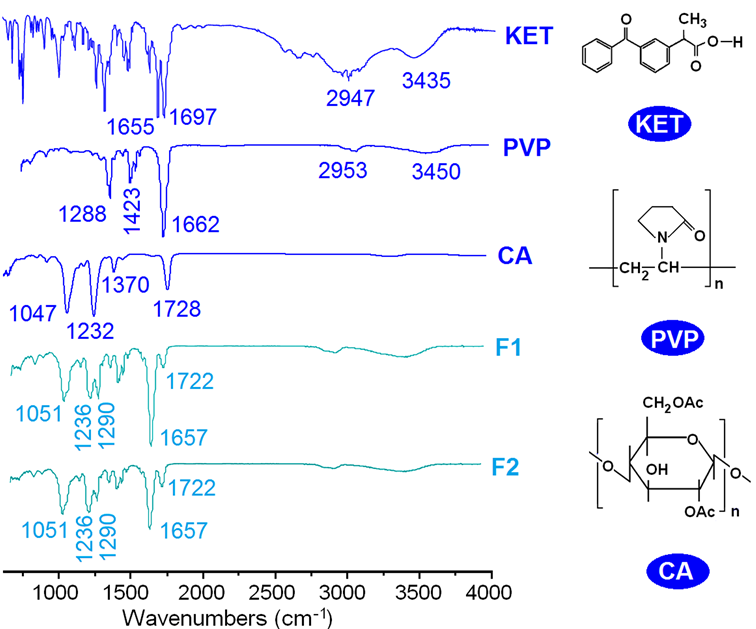
圖7.原料粉末(KET、PVP和CA)、核-殼納米纖維F1、三層核-殼納米纖維F2和原料的分子式的ATR-FTIR光譜。
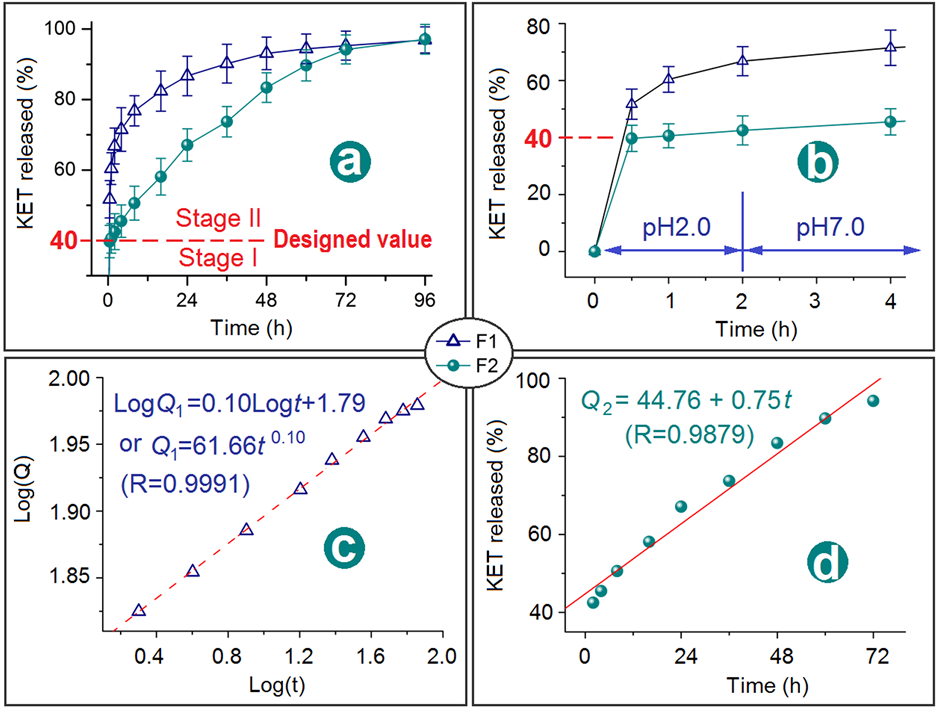
圖8.制備的納米纖維的雙階段釋放性能:(a)KET在整個時間段內隨時間的累積釋放百分比;(b)第一階段的藥物釋放;(c)第二階段從核-殼納米纖維F1中釋放KET的動力學;(d)第二階段從三層核-殼納米纖維F2中釋放KET的藥物釋放動力學。
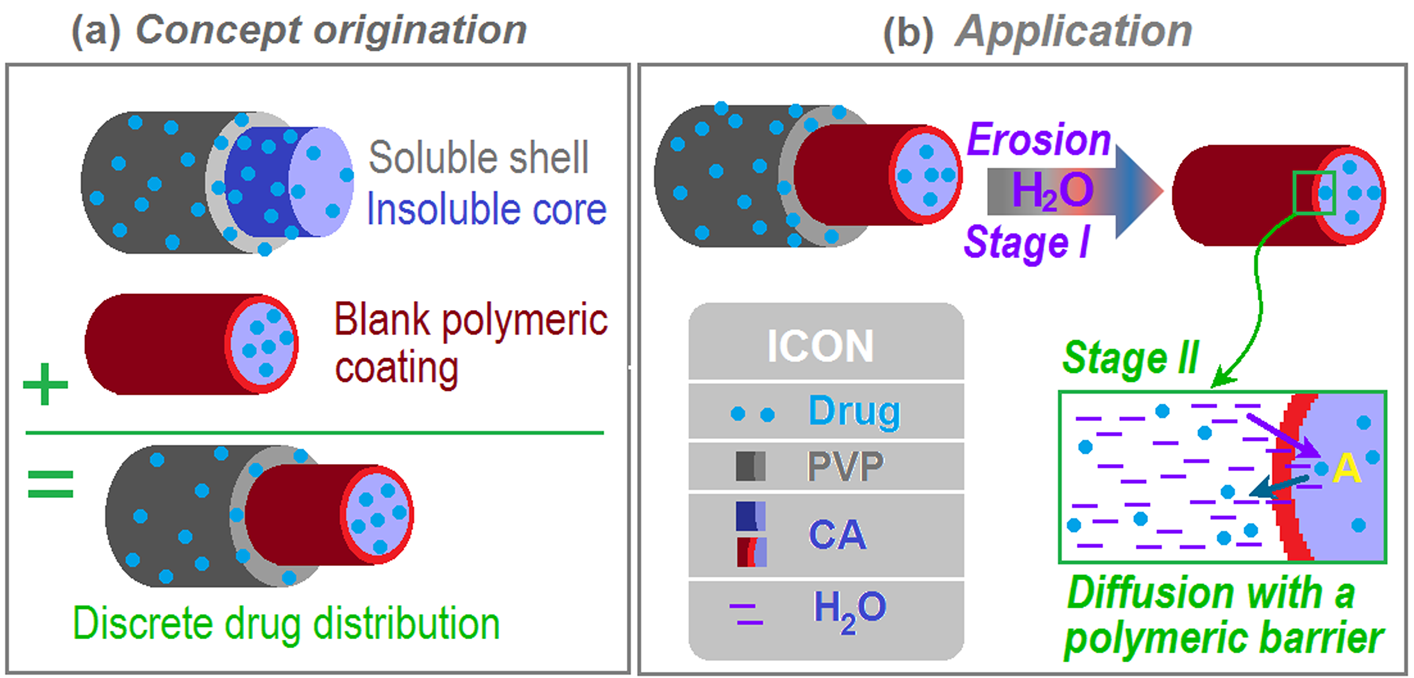
圖9.(a)具有離散藥物分布的三層納米纖維的起源,以及(b)多種藥物釋放機制的組合,以更好地應用雙階段藥物控釋。