DOI:10.1016/j.actbio.2019.12.038
在細胞友好的工藝條件下制備具有可調形貌的微/納米結構水凝膠,這將使針對特定生物醫學應用的水凝膠支架的合理設計成為可能。本文采用全水單步反應靜電紡絲法制備了納米級和微米級形貌可控的水凝膠網絡。酰肼和醛官能化的聚(低聚乙二醇甲基丙烯酸酯)(POEGMA)是由雙筒注射器和聚(環氧乙烷)(PEO)作為靜電紡絲助劑共紡而成。通過改變PEO和/或POEGMA的濃度和分子量,可以制備出各種形態,從純纖維到串珠狀纖維,再到具有可調珠徑的珠網絡形態,由于在凝膠結構內形成的動態共價交聯鍵,所有這些在水中均保持整體穩定。通過在納米級(即凝膠內的交聯密度)和微米級(即形成的網絡結構)上獨立控制凝膠形態,可以調整所得支架的溶脹、降解和力學的速率以及大小,相對于觀察到的力學和降解率,其具有非典型的獨立性溶脹。此外,證明了網絡的內部形態可以系統地改變支架內的細胞反應和從支架釋放蛋白質的速率,其中小纖維顯示出最佳的細胞增殖,串珠狀網絡表現出最慢的蛋白質釋放動力學和在靜電紡絲后保持很高的細胞活性,而串珠狀纖維表現出中等的性能。
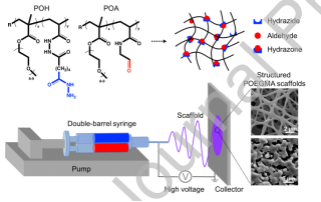
圖1.反應性靜電紡絲設置方案,以制備結構化的POEGMA水凝膠支架。

圖2.(A-B)用DIW洗滌(A)之前和之后(E)的7.5wt%POH/POA+2.5wt% 600PEO支架(600PEO2.5PO7.5)的光學圖像。(C-H)用DIW洗滌(24小時浸泡)之前(C,E,G)和(D,F,H)之后用不同濃度的聚合物前驅體制備的POH/POA+600PEO的SEM圖像。(I-M)使用與水凝膠反應性靜電紡絲相同的靜電紡絲條件對600PEO(無POH/POA)進行靜電紡絲的SEM圖像。
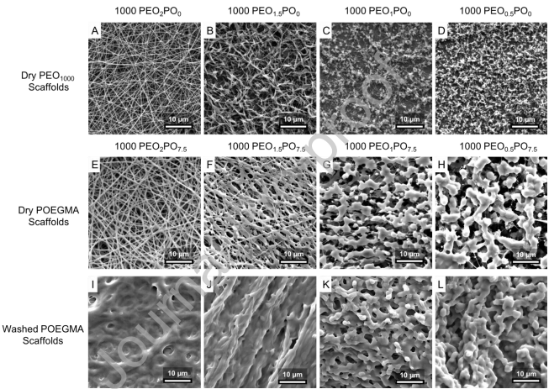
圖3.不含POH/POA的電紡 1000PEO(A-D)和含不同1000PEO濃度的POH/POA+1000PEO(E-H)支架的SEM圖像。(I-L)用DIW洗滌后,(E-H)中所示的電紡POH/POA+1000PEO支架的(I-L)SEM圖像。

圖4.用DIW浸泡(A-C)之前和之后(D-F)的POH/POA濃度為10 wt%的電紡水凝膠的SEM圖像。(A,D)POH/POA+600PEO(1 wt%);(B,E)POH/POA+1000PEO(1 wt%);(C,F)POH/POA+1000PEO(0.67 wt%)。
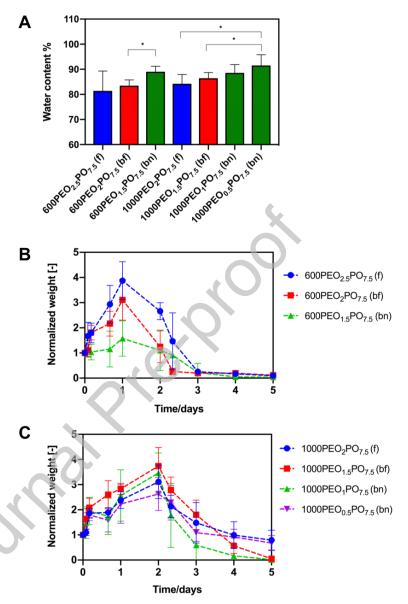
圖5.(A)用600PEG和1000PEG制備的POH/POA+PEO電紡支架在37℃的10 mM PBS中的溶脹。相對于在不同PEO濃度下制備的相應纖維凝膠結構,星號表示未配對t檢驗中p<0.05。(B-C)用600PEG(B)和1000PEG(C)制備的POH/POA+PEO電紡支架在37℃的1 M HCl中,在加速條件下測得的歸一化降解動力學。f、bf和bn代表產生的不同形態:纖維(f),串珠狀纖維(bf)或珠狀網絡(bn)。
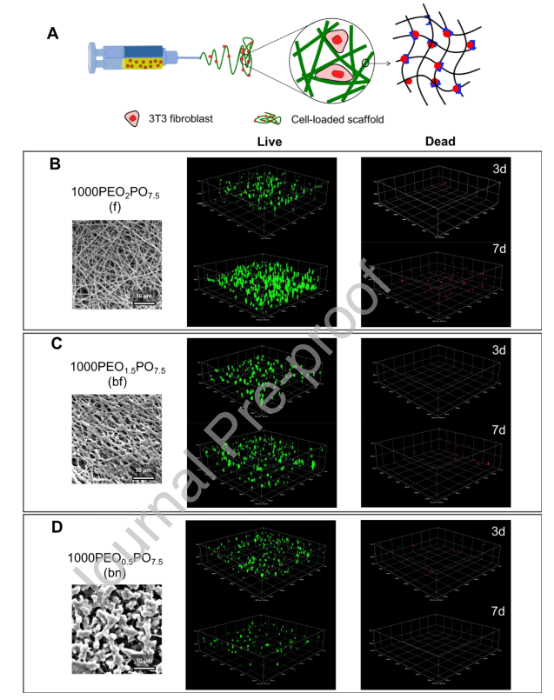
圖6.共電紡成具有不同形態的POEGMA支架的3T3成纖維細胞的共聚焦顯微鏡圖像。(A)細胞靜電紡絲以將細胞包封在支架中的方案;(B-D)具有不同形態的POH/POA+1000PEO,包括纖維(f)、串珠纖維(bf)和串珠網絡(bn)結構。活細胞用鈣黃綠素AM(488 nm,綠色)染色,死細胞用溴乙啡錠二聚體(546 nm,紅色)染色。3D共焦圖像的體積為1302μm×1302μm×355μm。
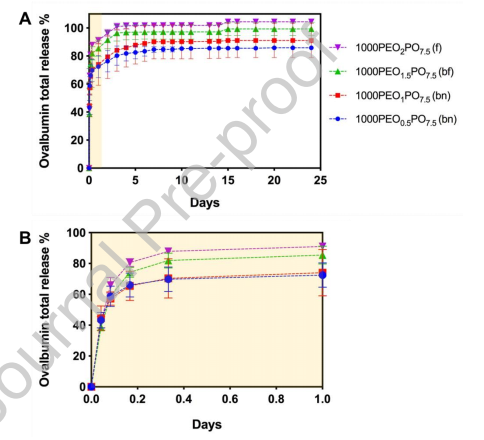
圖7.模型蛋白卵清蛋白的釋放動力學與用7.5 wt%POH/POA制備的1000PEO支架在24天之內的PEO濃度的關系(A);面板(B)僅顯示第一天的數據縮放,以更清楚地顯示不同形態之間的早期釋放動力學差異。 f =光纖,bf =串珠光纖,bn =珠網
 微信二維碼
微信二維碼