組織工程支架作為一種人工細胞外基質,可促進組織再生和修復。因此,支架的內部結構對細胞粘附、生長和遷移至關重要。在本文中,基于超臨界二氧化碳發泡技術,通過引入第二相聚乳酸靜電紡絲納米纖維,制備了一種由非均相納米纖維誘導的新型三維(3D)多孔聚己內酯/聚乳酸組織工程支架。掃描電鏡結果表明,所制備的支架具有明顯的納米纖維結構和3D網狀多孔結構。此外,還系統地探討了發泡溫度對孔隙形態的影響。拉伸試驗和水接觸角測量表明,新型支架具有良好的機械性能和親水性。橫斷面人臍帶內皮細胞(HUVEC)培養結果表明,該支架具有較好的生物相容性,能顯著促進HUVECs的粘附、遷移和通透性。單細胞遷移試驗表明3D多孔支架有效促進了HUVEC遷移。因此,3D多孔支架在血管補片領域具有巨大的應用潛力。
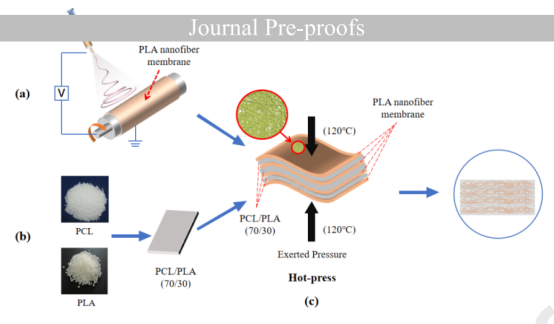
圖1.多層PCL/PLA復合膜的制備示意圖。
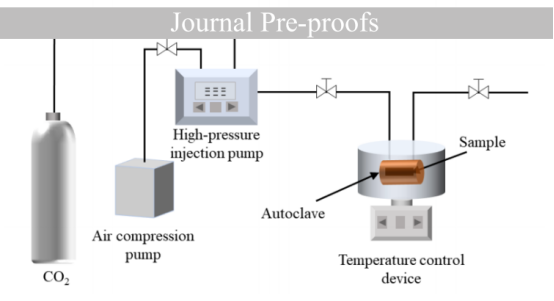
圖2.間歇微孔發泡工藝示意圖。

圖3.(a)不同支架的照片,(b-c)PLA纖維的SEM圖像和纖維直徑分布,(d)多層PCL/PLA復合膜的表面形貌,以及(e)多層PCL/PLA復合膜的橫截面形貌。

圖4.不同樣品形貌的SEM圖像:(a)發泡PCL/PLA(70/30)膜,(b)未發泡多層PCL/PLA復合膜,(c-d)發泡多層PCL/PLA復合膜。
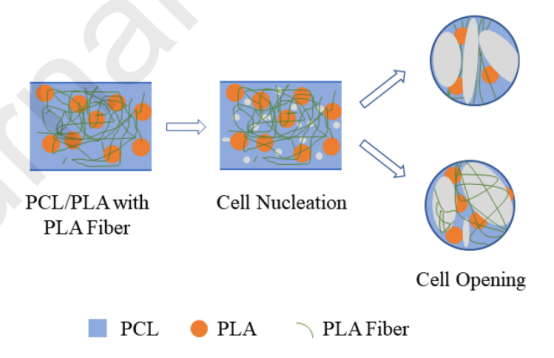
圖5.網狀孔隙結構形成示意圖。
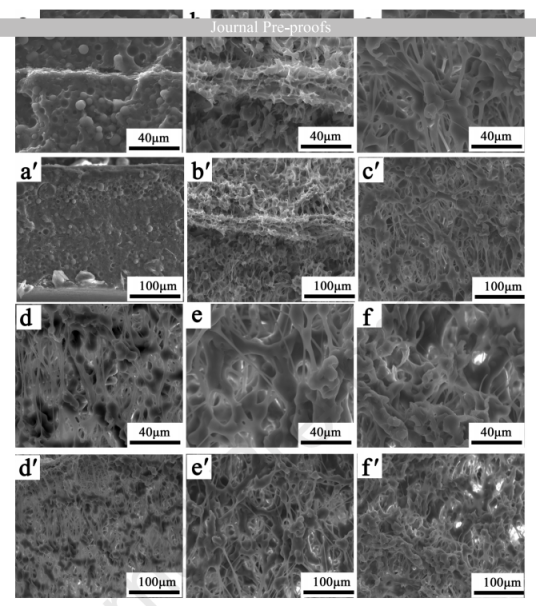
圖6.復合膜的橫截面以及不同溫度發泡的復合材料的形貌:(a)和(a')未發泡,(b)和(b')45℃,(c)和(c')50℃,(d)和(d')55℃,(e)和(e')60℃,(f)和(f')65℃。
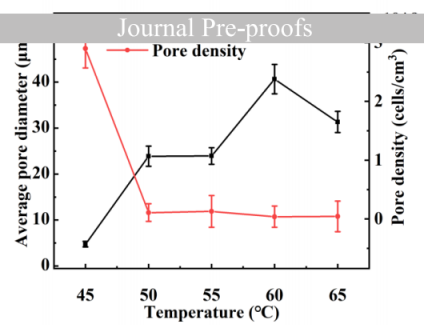
圖7.發泡溫度對微孔發泡多層PCL/PLA復合膜孔徑和密度的影響。
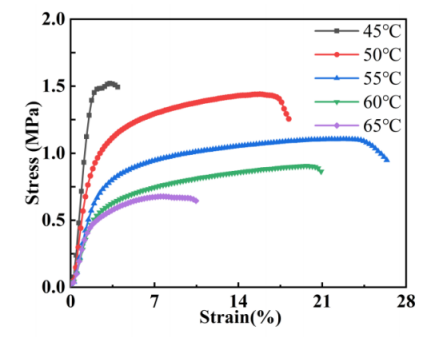
圖8.不同溫度發泡的多層PCL/PLA復合膜的應力-應變曲線。
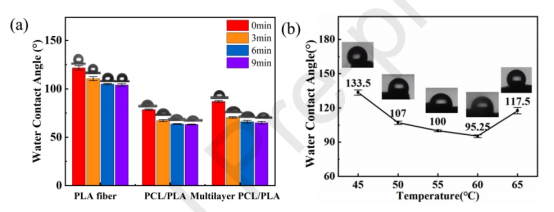
圖9.(a)PLA纖維對PCL/PLA(70/30)薄膜WCA的影響;(b)不同溫度發泡的多層PCL/PLA復合膜的WCA(*:p<0.5)。
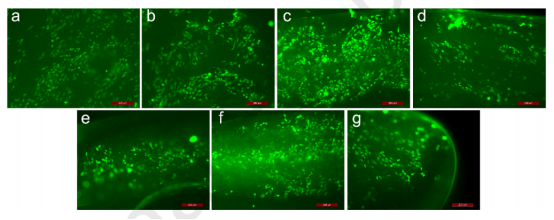
圖10.不同樣品的細胞活性:(a)PLA纖維;(b)發泡的PCL/PLA(70/30)薄膜;(c-g)不同溫度下發泡的多層PCL/PLA復合膜,包括45℃、50℃、55℃、60℃和65℃。
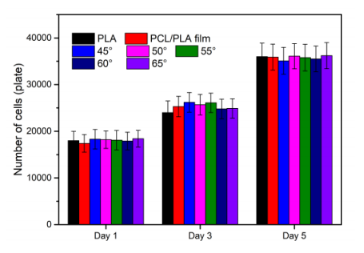
圖11.第1、3和5天不同樣品中的CCK-8細胞增殖:PLA纖維、發泡PCL/PLA(70/30)薄膜和發泡多層PCL/PLA復合材料。
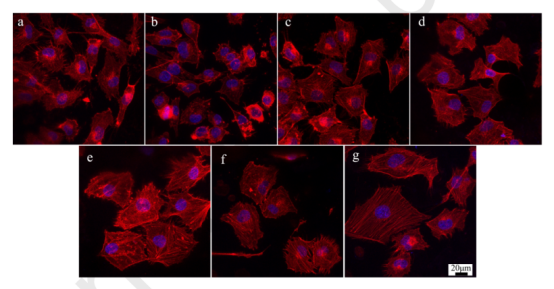
圖12.不同樣品的HUVEC形態:(a)PLA纖維;(b)發泡PCL/PLA(70/30)薄膜;(c-g)不同溫度發泡的多層PCL/PLA復合膜,包括45℃、50℃、55℃、60℃和65℃。

圖13.HUVEC在不同樣品上的粘附和遷移:(a)PLA纖維;(b)發泡PCL/PLA(70/30)薄膜;(c-g)不同溫度發泡的多層PCL/PLA復合膜,包括45℃、50℃、55℃、60℃和65℃。
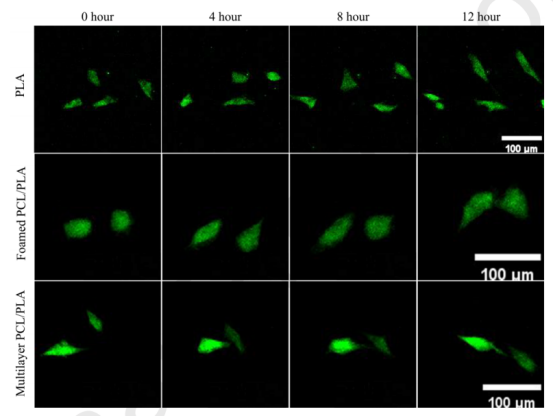
圖14.HUVEC在不同樣品上的遷移:(a)PLA纖維;(b)發泡PCL/PLA(70/30)薄膜;(c)發泡多層PCL/PLA復合膜。
 微信二維碼
微信二維碼