DOI:10.1016/j.msec.2020.111738
生物分子載體結構由于其在骨組織工程領域的潛在應用而引起了人們的極大關注。在這項研究中,首次開發了可控釋BMP-6的MOF嵌入電紡纖維支架,以增強骨再生功效。首先,將BMP-6包封ZIF-8納米晶體作為生長因子分子的新型載體,進行一步快速結晶,然后靜電紡絲由聚(ε-己內酯)和BMP-6包封ZIF-8納米晶體組成的混合溶液,從而制備出納米纖維支架。經計算,ZIF-8納米晶體的BMP-6分子包封率為98%。體外研究表明,BMP-6的生物活性得以保留,釋放時間長達30天。釋放動力學符合Korsmeyer-Peppas模型,表現出偽Fickian行為。體外成骨研究表明BMP-6緩釋對MC3T3-E1前成骨細胞的成骨分化有明顯的促進作用。此外,體內研究還顯示BMP-6的持續緩慢釋放是導致大鼠顱骨缺損中礦化良好的新骨形成的原因。該研究結果證實嵌入MOF載體的電紡支架可以用作骨組織工程應用中骨再生的有效平臺。所提出的方法適用于不同組織工程應用中的各種生長因子分子。
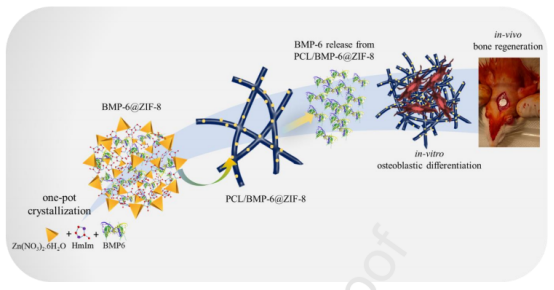
圖1.BMP-6@ZIF-8的一步結晶和PCL/BMP-6@ZIF-8電紡纖維支架的制備示意圖,該支架用于控釋BMP-6以體外誘導成骨細胞分化和體內骨再生。
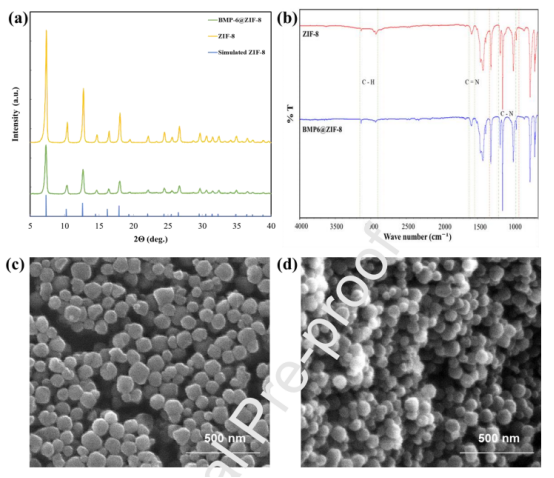
圖2.ZIF-8和BMP-6@ZIF-8納米晶體的表征。ZIF-8、BMP-6@ZIF-8和模擬ZIF-8的PXRD峰(a),ZIF-8和BMP-6@ZIF-8的FTIR-ATR光譜(b),ZIF-8(c)和BMP-6@ZIF-8(d)的SEM圖像。
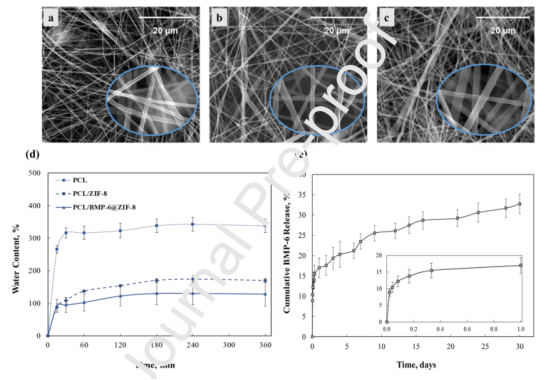
圖3.PCL、PCL/ZIF-8和PCL/BMP-6@ZIF-8膜的特性。PCL(a),PCL/ZIF-8(b)和PCL/BMP-6@ZIF-8(c)纖維的SEM圖像。插圖顯示放大20000倍的圖像。電紡膜的保水率和水含量(%)(d)。通過酶聯免疫吸附試驗測定PCL/BMP-6@ZIF-8纖維膜的BMP-6體外釋放曲線(e)。插圖顯示24小時內的釋放曲線。
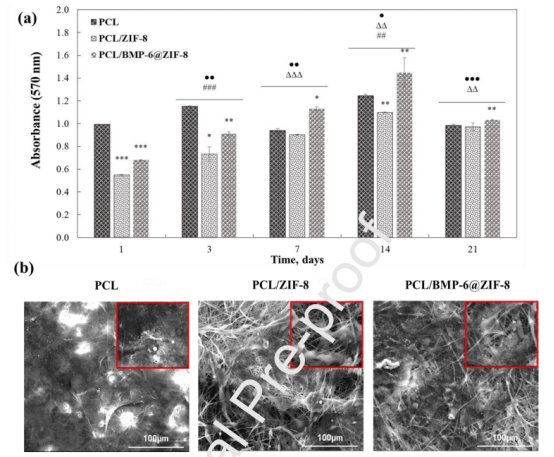
圖4.通過Presto Blue分析檢測PCL、PCL/ZIF-8和PCL/BMP-6@ZIF-8膜上的細胞增殖。以PCL為對照,n=4,*p<0.05,**p<0.01,***p<0.005;對于PCL,##p<0.01;對于PCL/ZIF-8,ΔΔp<0.01,ΔΔΔp<0.005;以第一天的PCL/BMP-6@ZIF-8為對照,·p<0.05,··p<0.01和···p<0.005。在PCL、PCL/ZIF-8和PCL/BMP-6@ZIF-8膜上培養14天的MC3T3-E1細胞的SEM圖像(b)。插圖顯示放大4000倍的圖像。
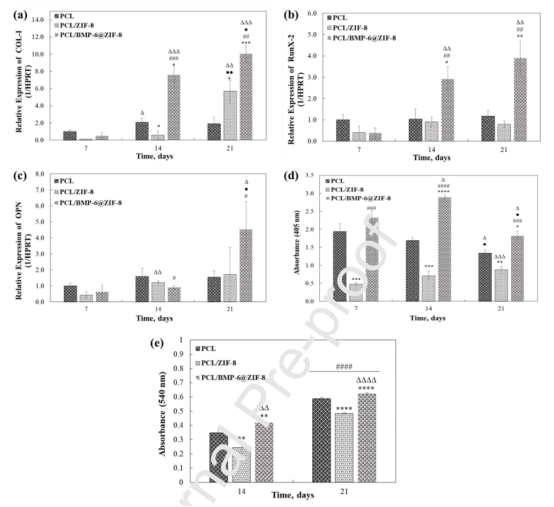
圖5.通過定量RT-PCR測量在膜上培養的MC3T3-E1細胞中成骨相關基因的表達。COL-1(a),RunX2(b)和OPN(c)。在膜上培養的細胞的定量ALP活性(d)。當對照組為PCL時,n=3,*p<0.05,**p<0.01,***p<0.005;當對照組為PCL/ZIF-8時,#p<0.05,##p<0.01,###p<0.005;當對照組為第7天時,Δp<0.05,ΔΔp<0.01,ΔΔΔp<0.005;而當對照組為第14天時,·p<0.05,··p<0.01,···p<0.005。比色定量結果顯示細胞在PCL、PCL/ZIF-8和PCL/BMP-6@ZIF-8膜上培養14天和21天的基質礦化,由ARS進行染色(e)。當對照組為PCL時,**p<0.01,***p<0.005,****p<0.001;當對照組為PCL/ZIF-8時,ΔΔp<0.01,ΔΔΔΔp<0.001;當對照組為第7天時,####p<0.001。
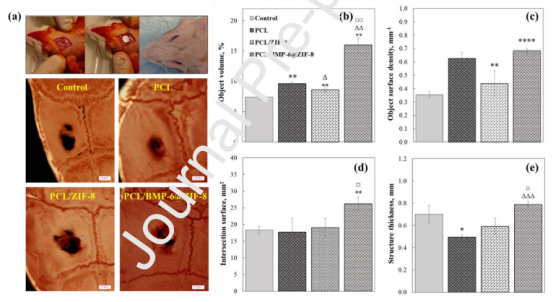
圖6.建立Wistar大鼠顱骨臨界缺損的手術方法,植入PCL/BMP-6@ZIF-8膜以及8周后的愈合傷口部位(n=6)。Micro-CT圖像顯示8周后的缺損部位。深色區域對應于未愈合的骨缺損區域。對于植入PCL/BMP-6@ZIF-8膜的部位,可以觀察到新骨形成,比例尺=1mm(a)。從顯微CT圖像評估物體體積百分比(b),物體表面密度(c),相交表面(d)和表面厚度值(e)。當PCL為對照時,Δp<0.05,ΔΔp<0.01,ΔΔΔp<0.005;當PCL/ZIF-8為對照時,□p<0.05和□□p<0.01。
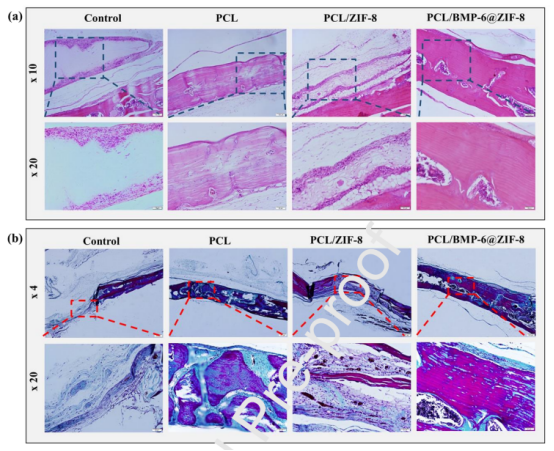
圖7.植入8周后,修復骨缺損的H&E染色(a)和Masson三色染色(b)。
 微信二維碼
微信二維碼