DOI: 10.1021/acsnano.0c03981
再生工程作為一種成功的策略,通過融合多個領域的專業知識,實現復雜組織和生物器官的再生。這種創新的突破性方法刺激了人們對具有獨特生物識別特性的生物材料的更多選擇性需求。理想的生物材料能夠很好地模擬天然組織細胞外基質(ECM)的分層結構和特征。納米制備技術為納米纖維支架的開發提供了極好的跳板,該支架可以在直接的細胞環境中產生積極的相互作用,并在分子水平上刺激特定的再生級聯反應,從而產生健康的組織。本文系統綜述了靜電紡絲技術及其在基于基質的再生工程中的應用,主要集中于肌肉骨骼組織。此外,還簡述了靜電紡絲/3D打印系統的雙重性,并對納米纖維基質的技術前景和未來方向進行了探討。
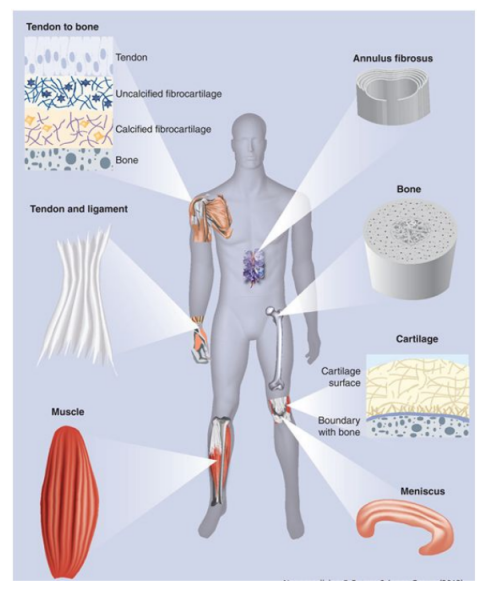
圖1.在不同的骨骼肌肉組織中發現的膠原蛋白納米纖維的組織。肌腱和韌帶組織由單軸排列且呈波浪形的膠原蛋白納米纖維組成。膠原纖維在肌腱到骨的插入部位表現出從定向到隨機的取向,在彎月面和纖維環中呈圓周排列。軟骨組織中的膠原纖維呈分層排列。
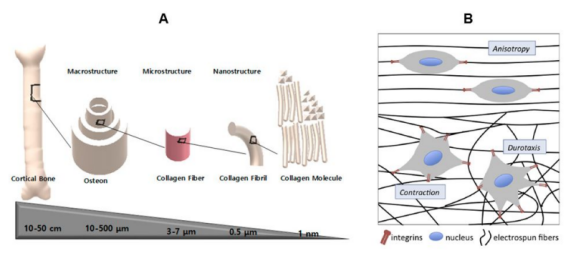
圖2.(A)顯示骨骼的層次化宏觀結構構造和骨的圓柱形結構以及膠原蛋白的微結構/納米結構。(B)細胞-納米纖維相互作用的示意圖,顯示了在整合素的幫助下細胞骨架對纖維的附著。纖維的各向異性排列和排列會影響細胞的形態,并且當細胞與基質的柔軟區域接觸時,細胞會顯示收縮,因此基質的硬度會調節細胞的遷移(趨硬行為)。
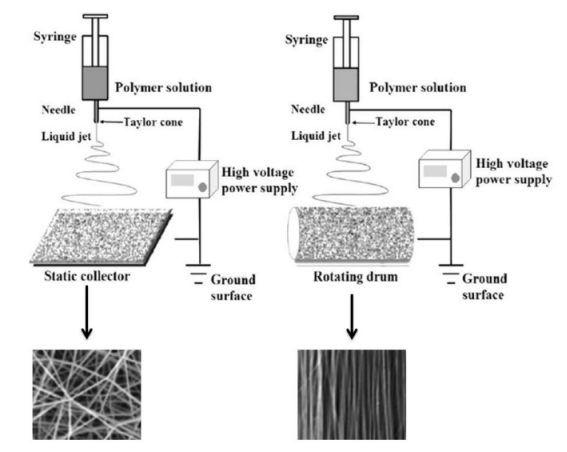
圖3.帶有靜態收集器和旋轉收集器的靜電紡絲工藝示意圖。隨機取向的納米纖維被收集在靜態收集器上,而滾筒則產生單軸排列的納米纖維。
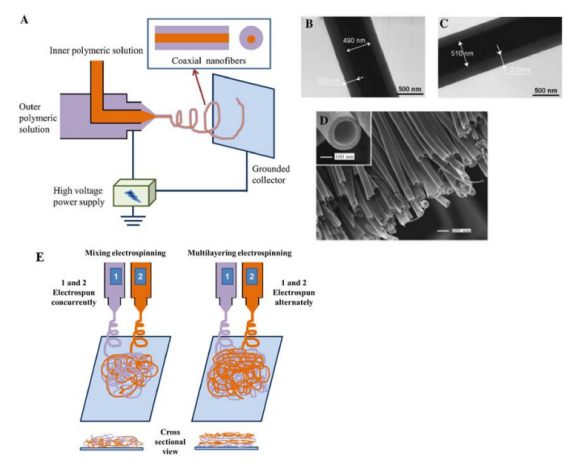
圖4.同軸、混合和多層靜電紡絲系統的圖解說明。(A)同軸靜電紡絲,涉及通過內外針同軸噴絲頭擠出兩種不同的聚合物溶液,(B和C)同軸電紡納米纖維的透射電子顯微鏡圖像,(D)中空納米纖維的微觀視圖。(E)分別使用混合和多層靜電紡絲工藝制備的混合和多層納米纖維。
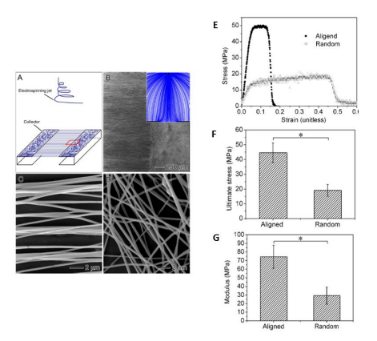
圖5.定向至隨機取向的電紡納米纖維。(A)用于制備定向至隨機納米纖維支架的實驗裝置,(B)SEM圖像顯示了隨機和單軸排列的PLGA,左側為隨機取向,而右側為定向排列,(C-D)具有高放大倍數的無規和定向纖維視圖,(E-G)定向和無規納米纖維支架的機械性能。定向納米纖維具有較高的模量和極限應力。
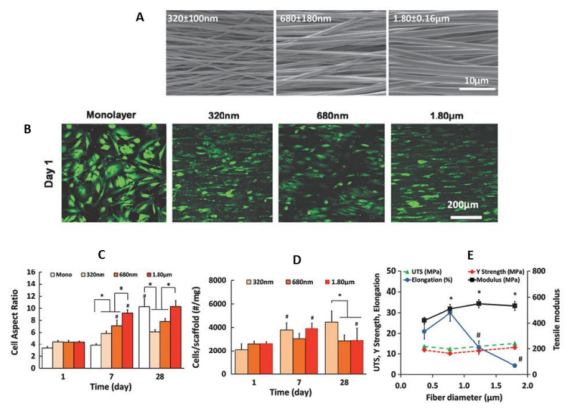
圖6.纖維直徑對支架細胞活性和機械性能的影響。(A)不同直徑的納米和超細纖維的SEM圖像,(B)支架上的活/死細胞活力測定,(C)細胞長徑比的時間依賴性變化。(D)細胞增殖隨培養時間的變化,(E)拉伸性能隨直徑的變化。
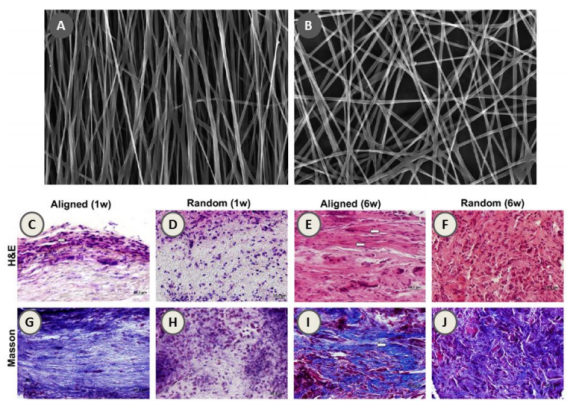
圖7.PLLA的電紡納米纖維。(A)定向納米纖維和(B)隨機取向納米纖維支架的SEM圖像,(C-F)納米纖維誘導組織形成的蘇木精-伊紅染色組織學研究,(G-J)Masson三色染色顯示在定向和隨機纖維支架上形成膠原纖維。

圖8.3D打印和靜電紡絲技術的融合。(A)在打印過程中,在適當的層上進行靜電紡絲制備具有網孔(15s、30s、45s和120s的網孔密度)且均勻分布的雙尺度支架。(B)3D打印支架和具有電紡納米纖維的雙尺寸支架的SEM圖像。在打印過程中將納米纖維直接電紡到支架上,可獲得雙尺寸支架(比例尺=300μm)。(C)3D打印支架和3D復合支架的照片和SEM圖像。通過將分散的納米纖維注入3D打印支架網孔中(比例尺=1mm)可獲得復合支架。
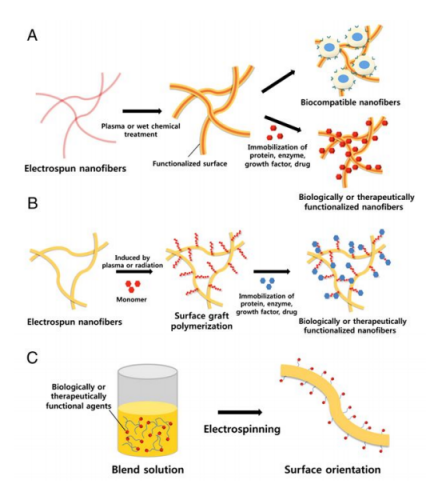
圖9.顯示將生物活性分子整合到納米纖維中的不同修飾方法的示意圖。(A)通過等離子體處理,(B)通過表面接枝聚合固定生物活性分子,(C)基底和生物活性劑的共同靜電紡絲。
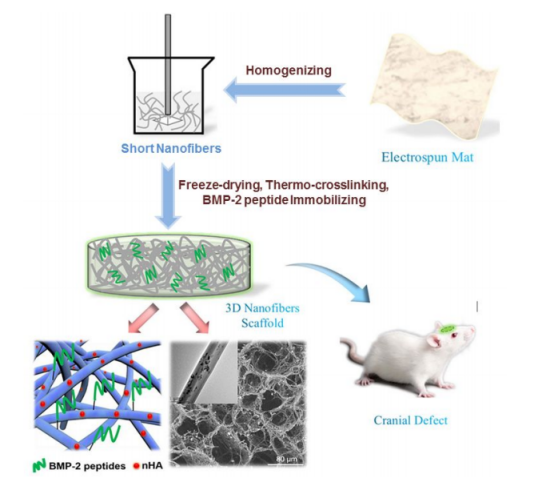
圖10.制備三維(3D)電紡納米纖維支架用于大鼠顱骨缺損模型的骨組織再生。